دررفتگی مادرزادی مفصل ران به دوران بقراط باز میگردد. این بیماری که به دیسپلازی هیپ یا دیسپلازی تکامل هیپ (DDH) نیز شناخته میشود، صدها سال است که تشخیص و درمان میشود. از معروفترین آنها میتوان به اورتولانی (Ortolani) پزشک ایتالیایی اشاره کرده که در قرن 19، دیسپلازی هیپ را ارزیابی، تشخیص و شروع به درمان میکرد. گالئازی (Galeazzi) بعدها بیش از 12000 مورد DDH دارای شواهد کوتاه شدن فمور در حالت فلکشن و دررفتگی هیپ، را گزارش کرد. از آن زمان، پیشرفت شایانی در ارزیابی و درمان DDH صورت گرفته است.
هنوز در سطح جهانی در ارتباط با اصطلاح DDH به اتفاق نظر نرسیدهاند. به طور معمول، اصطلاح DDH به بیماران متولد شده به همراه دررفتگی و بیثباتی هیپ که در نهایت به دیسپلازی هیپ ختم میگردد، اطلاق میشود. به طور گستردهتر، DDH به هر گونه رشد غیر طبیعی هیپ گفته میشود. رشد غیر طبیعی هیپ ساختارهای استخوانی همانند؛ استابولوم و قسمت پروگزیمال فمور به همراه لابروم، کپسول و دیگر اجزای بافت نرم را شامل میشود. این بیماری ممکن است در هر زمانی، از همان آغاز دوران بارداری گرفته تا تکامل سیستم اسکلتی ایجاد شود. به منظور دقت و سادگی بیشتر استفاده از اصطلاح دیسپلازی هیپ ترجیح داده میشود. عموما، این اختلال به دررفتگی مادرزادی هیپ اشاره دارد.
اصطلاحات دقیقتری برای توصیف واضحتر بیماری استفاده میشوند، به قرار زیر هستند:
- Subluxation – اتصال ناقص سطح غضروفی سر فمور و استابولوم
- Dislocation – دررفتگی کامل سطح غضروفی سر فمور از حفره استابولوم
- Instability – دررفتگی کامل یا ناقص هیپ با دست کاری
- Tetralogic dislocation – دررفتگی هیپ پیش از تولد
تشخیص به موقع مهمترین مسئله در درمان کودکان مبتلا به DDH است. استفاده از سونوگرافی و دیگر تجهیزات تصویربرداری تشخیصی به همراه برنامههای آموزشی برای بالا بردن سطح آگاهی، در حل این مسئله راهگشا خواهد بود. به تازگی، روشهای کمتر تهاجمی (مثل؛ تکنیکهای اندوسکوپی و جراحی با گاید تصویری) برای کاهش مرگ و میر ناشی از جراحی و تسریع روند بهبود، توسعه یافتهاند.
پاتوفیزیولوژی
DDH رشد غیر طبیعی هیپ را شامل میشود. اعتقاد بر این است سستی لیگامانی با دیسپلازی هیپ مرتبط مییاشد؛ با این حال این ارتباط به طور قطع واضح نیست. DDH جزو اختلالات مرتبط با شلی لیگامانی مثل، سندروم اهلرز دانلوس یا سندروم مارفان طبقهبندی نمیشود.
معمولا کودکان در هنگام تولد شلی لیگامانی دارند با این حال ران آنها بیثبات نیست، در واقع برای دررفتگی ران کودک نیروی زیادی نیاز است. بنابراین تنها برای DDH شلی لیگامانی کافی نیست. در بدو تولد، حفره استابولوم نوزادان سفید پوست کم عمقتر است، در این دوره قرارگیری نامناسب هیپ یا دورهی کوتاهی از شلی لیگامانی به دررفتگی هیپ منجر خواهد شد. با این حال این ویژگی در کودکان آفریقایی تبار که میزان DDH در آنها کمتر است، صدق نمیکند.
اتیولوژی
اتیولوژی دیسپلازی هیپ واضح نیست اما این بیماری با عوامل مختلفی مرتبط است. یکی از این عوامل پیشزمینه نژادی ست: شیوع دیسپلازی هیپ در آمریکاییهای اصیل و لاپلندیها (25-50 مورد در هر 1000 نفر) بیشتر از دیگر نژادها است و شیوع در چینیهای جنوبی و سیاه پوستان بسیار اندک میباشد. زمینهی ژنتیکی نیز در این بیماری مؤثر است به این صورت که احتمال بروز دیسپلازی در فرزندان والدین با سابقهی DDH نسبت به همتایان خود 10 برابر بیشتر است.
دیگر عوامل احتمالی مرتبط با DDH شامل پوزیشن درون رحم و جنسیت است، برخی از این عوامل با یکدیگر همبستگی دارند. جنسیت مؤنث، فرزند اول و جایگیری بریچ با افزایش شیوع DDH مرتبط است. 80 درصد تخمینی مبتلایان به DDH مؤنث هستند و نسبت جایگیری بریچ در کودکان مبتلا به DDH تقریبا 20 درصد است (در مقایسه با 2-4 درصد در جمعیت عمومی). در برخی مطالعات، شیوع DDH در نوزادان مؤنث متولد شده با جایگیری بریچ، در حدود 1 مورد در هر 15 نفر گزارش شده است.
دیگر اختلالات موسکولواسکلتال مانند فشردگی و جایگیری نامنااسب درون رحمی مثل؛ متاتارسوس اداکتوس و تورتیکولیس همچنین الیگوهیدروآمنیون نیز با افزایش شیوع DDH مرتبط گزارش شده است. DDH هیپ چپ شایعتر از هیپ راست میباشد ممکن است جایگیری معمول درون رحمی هیپ چپ در مقابل ساکروم مادر باعث وضعیت اداکت در هیپ شده و دلیل این اتفاق باشد. در جوامعی که قنداق بستن در آنها مرسوم باشد به علت فشار بر هیپ نوزاد به صورت اداکت، شیوع دسپلازی هیپ در آنها بالاتر است.
دیسپلازی هیپ ممکن است با اختلالات نوروماسکولار زمینهای مثل، سربرال پالسی، میلومنینگوسل، آرتروگریپوزیس و سندروم لارسن ( که معمولا این موارد DDH شناخته نمیشوند)، مرتبط باشد.
اپیدمیولوژی
شیوع کلی DDH تقریبا 1 مورد در هر 1000 نفر گزارش شده است، با این حال بارلو (Barlow) معتقد بود بروز بیثباتی هیپ طی آزمایش نوزادان تازه متولد شده در حدود 1 مورد در هر 60 تولد زنده بوده است. طبق مطالعهی بارلو بیش از 60 درصد از تازه متولد شدههای با بیثباتی هیپ، پس از 1 هفته ثابت شدند و 88 درصد طی 2 ماه ثابت شده بودند، 12 درصد باقیمانده (1 در هر 60 تازه متولد شده یا 0.2 درصد کل) بیثباتی هیپ در آنها پایدار بود.
پیشآگهی
در کل پیشآگهی کودکان درمان شدهی دیسپلازی هیپ، به خصوص در صورت درمان بدون جراحی، بسیار خوب است. اگر درمان بدون جراحی موفقیتآمیز نبود و نیاز به جراحی داشت، نتیجه کمتر دلخواه خواهد بود، هر چند نتیجه در کوتاه مدت رضایتبخش است. اگر برای درمان نیاز به عملیات ثانویهای باشد، نتیجهی کلی به طور قابل ملاحظهای بد خواهد بود.
برخی ازنویسندگان معتقدند به دلیل تشخیص دیر هنگام و اقدامات درمانی بزرگتر، پیشآگهی کودکان با دیسپلازی هیپ دو طرفه ضعیف است. در مطالعهای روی کودکان در سن راه رفتن، گروهی با دررفتگی دو طرفهی هیپ و گروه دیگر با دررفتگی یک طرفهی هیپ که هر دو گروه تحت جراحی و اوستئوتومی پلویک همراه با یا بدون استوئوتومی فمورال قرار گرفته بودند مقایسه شدند؛ نتایج رادیوگرافی هر دو گروه یکسان بود.
در این مطالعه، میزان استئونکروز در گروه دو طرفه بالاتر بود اما این مسئله با توجه به سن بیشتر و دررفتگی شدیدتر هیپ پیش از جراحی، توجیه شد. نویسندگان نتیجه گرفتند که دلیل پیشآگهی بد کودکان با دررفتگی هیپ دو طرفه، نتیجهبخشی غیر قرینهی درمان میباشد.
درمان DDH
پاولیک هارنس
کودکان تشخیص داده شده در اوایل تولد معمولا با “پاولیک هارنس” تحت درمان قرار میگیرند. این روش ضمن ثابت نگه داشتن هیپ کودک، رشد طبیعی را امکان میسازد.
هارنس باید به صورت مداوم به مدت چندین هفته پوشیده شود و تنها توسط متخصص در آورده شود. هارنس طی جلسات فالواپ تنظیم شده و کلینیسین پیشرفت درمان کودک را به والدین توضیح خواهد داد.
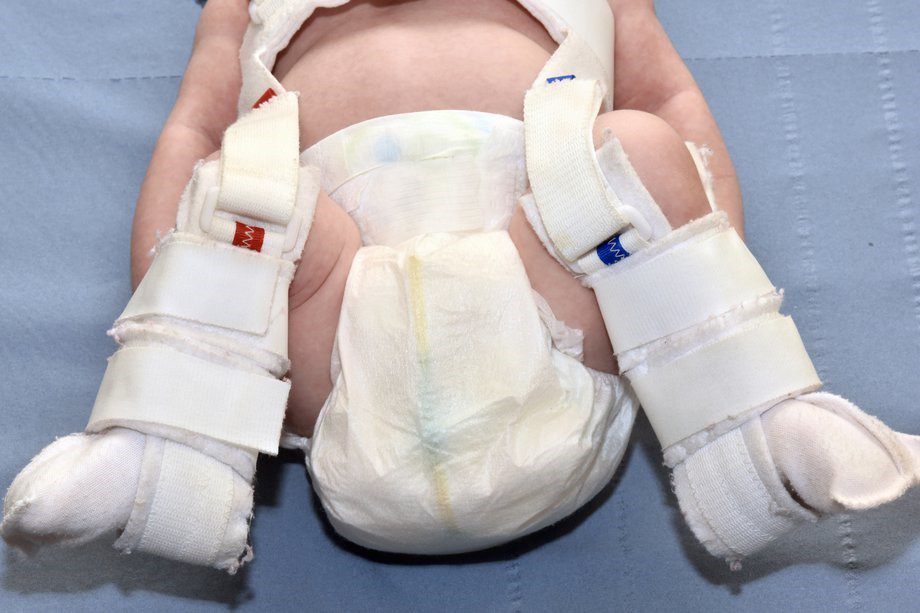
بیمارستان اطلاعات لازم برای مراقبت از کودک طی دورهی درمان با پالویک هارنس را در اختیار والدین قرار میدهد که به قرار زیر خواهد بود:
- چگونه بدون در آوردن هارنس لباسهای کودک را عوض کنید – پوشک حالت معمول پوشیده خواهد شد.
- در صورت کثیف شدن هارنس – نباید در آورده شود، اما میتوان با مواد ضد عفونیکننده و مسواک یا براش کهنه آن را تمیز کرد.
- وضعیت کودک در هنگام خواب – باید به جای پهلو به پشت خوابانده شوند.
- چگونه از حساسیتهای پوستی ناحیه بندهای هارنس جلوگیری کنید – توصیه خواهد شد تا پارچهای نرم و تمیز را دور بندها بپیچید.
در نهایت تا زمان در آوردن کامل هارنس، توصیه خواهد شد تا در دورههای کوتاهی در آورده و عوض شود. پس از در آوردن هارنس، کودک میتواند آزادانه حرکت کند و شنا توصیه خواهد شد.
جراحی
در صورت تشخیص DDH پس از 6 ماهگی یا کارایی نداشتن پالویک هارنس، نیاز به جراحی خواهد بود. معمولترین تکنیک جراحی ریداکشن نامیده میشود در این روش سر فمور درون کاسهی مفصل هیپ جا انداخته میشود.
جراحی تحت بیهوشی عمومی به یکی از دوو روش زیر صورت خواهد گرفت:
- Closed Reduction – سر فمور بدون برش بزرگ درون کاسهی مفصلی جا انداخته میشود.
- Open Reduction – برای جا انداختن سر فمور در کاسهی مفصلی جراح ناحیه کشاله ران را برش خواهد زد.
به مدت 6 ماه پس از جراحی هیپ کودک گچ گرفته خواهد شد. پس از مدتی برای اطمینان از روند درمان و ثابت ماندن هیپ، دوباره تحت بیهوشی عمومی مورد بررسی قرار میگیرد، پس از این بررسی هیپ برای ثابت شدن کامل به مدت 6 هفتهی دیگر دوباره گچ گرفته میشود.
بعضی از کودکان علاوه بر ریداکشن همان موقع یا پس از مدتی برای تصحیح هر گونه دفرمیتی استخوانی، نیاز به جراحی استخوان (استئوتومی) خواهند داشت.
پیشگیری DDH
باید به خاطر داشته باشیم که DDH قابل پیشگیری نبوده و هیچ کس در این مورد مقصر نیست. مفاصل ران کودکان به مدت کوتاهی پس از تولد بسیار منعطف خواهند بود.
با این حال در صورت قنداق بستن کودک، رشد ران کند شده و در خطر DDH خواهد بود. استفاده تز روشهای قنداق بستن که در آن مفاصل ران برای حرکت آزاد هستند، میتواند خطر دفورمیتی را کاهش دهد.
